Не в фарме: чем опасен отказ от исследований западных лекарств в России
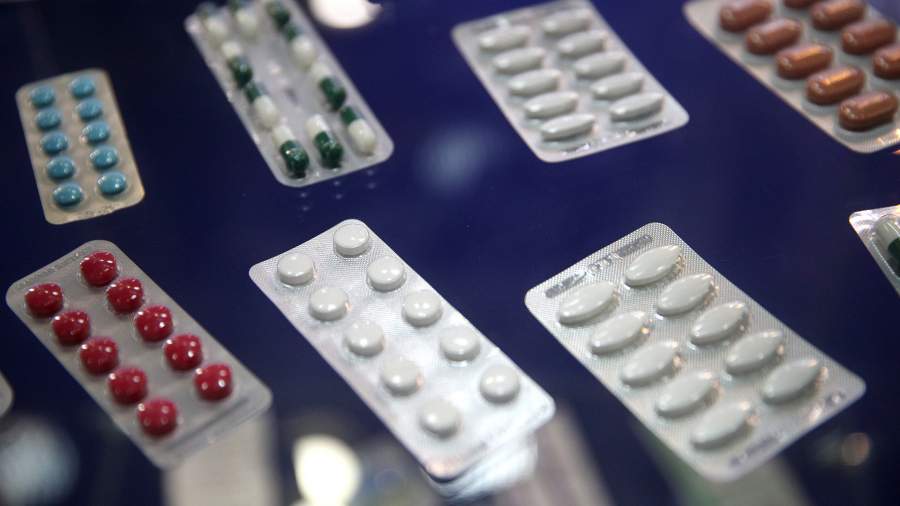
Некоторые западные фармкомпании отказались проводить клинические исследования новых препаратов в России. Pfizer в одном из заявлений допустил сворачивание и текущих испытаний. По оценкам экспертов, иностранные компании проводят в России порядка 600–700 испытаний, в них участвуют десятки тысяч человек. Резкая отмена или смена препарата может негативно отразиться на здоровье пациента, участвующего в исследовании, говорят врачи. «Известия» разбирались, какие последствия могут быть у решения западных фармкомпаний.
Закончить начатое
В России в настоящее время идет от 600 до 700 международных клинических исследований (КИ) новых медицинских препаратов, сообщила «Известиям» исполнительный директор Ассоциации организаций по клиническим исследованиям Светлана Завидова. Проведение части из них может оказаться под вопросом: международные фармацевтические компании Pfizer, Lilly, AbbVie, Sanofi, MSD, Novartis и ряд других заявили, что больше не будут проводить КИ своих разработок в России. Клинические исследования на реальных пациентах начинаются уже на заключительных стадиях испытаний новых лекарственных средств. Они проводятся, чтобы оценить эффективность и безопасность препарата. Число участников КИ может варьироваться от десяти до нескольких тысяч.
По оценке Светланы Завидовой, в текущих исследованиях задействовано несколько десятков тысяч человек. Для них завершение начатых КИ — принципиально важный вопрос, так как резкая отмена или смена препарата может негативно отразиться на здоровье пациента, участвующего в исследовании. Естественно, снабжает участников лекарствами их производитель, поэтому его отказ от продолжения исследований чреват отсутствием у пациента препарата, еще не поступившего в продажу.Большинство западных фармгигантов подчеркивает, что их решение затронет только новые клинические исследования. А все начатые ранее испытания будут завершены.
«Клинические исследования лекарственных препаратов на территории нашей страны продолжаются в соответствии с протоколами», — говорится в официальном ответе Минздрава на запрос «Известий».
Возможность для разных интерпретаций дала только позиция американской компании Pfizer.
Смена позиций
В середине марта Pfizer в англоязычной версии своего сайта выпустила заявление о деятельности компании в России. В нем однозначно сказано, что «Pfizer будет работать с FDA (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США) и другими регуляторами, чтобы перенести все текущие клинические исследования на альтернативные площадки за пределами России».Через несколько дней на русскоязычной странице компании в интернете был опубликован комментарий, где утверждается: «Компания Pfizer продолжит поддерживать клинические центры, участвующие в текущих программах клинических исследований, и участников, уже включенных в данные исследования в России…» На запрос «Известий», в чем именно будет выражаться эта поддержка, в компании не ответили.
В одном из основных центров клинических исследований в нашей стране — Сеченовском университете — «Известиям» сообщили, что проводящиеся там КИ компании идут без изменений.
— У нас нет информации об отмене испытаний. Лично у меня идет исследование компании Pfizer, и оно продолжается. Все, кто включен в исследование, продолжают участие, — отметила руководитель Центра клинического изучения лекарственных средств Сеченовского университета Елена Смолярчук.
В то же время даже решение фармкомпаний продолжить текущие исследования не гарантирует, что они будут завершены. Главная проблема — логистическая, пояснила Елена Смолярчук. Для завершения уже начатых клинических испытаний иностранным производителям предстоит завезти в Россию расходные материалы и сами лекарства. А затем доставить биообразцы участников исследования в центральные лаборатории, которые чаще всего расположены в Европе. При этом по правилам некоторых испытаний биоматериалы, например кровь, нужно отправлять в очень сжатые сроки. Как соблюдать эти условия, когда отсутствует авиасообщение между странами, остается неясным.Специалист добавила, что в договорах участников исследований прописано, что спонсор в одностороннем порядке может по разным причинам прекратить их. Если это случится, то юридически Pfizer не будет иметь никаких обязательств перед участниками. Кроме того, прекращение исследования всегда можно объяснить тем, что фармацевты уже накопили достаточное количество случаев лечения препаратом для полноценных научных выводов.
Без обязательств
О том, что с формальной точки зрения фармацевтические компании легко могут прервать текущие клинические исследования в России, также рассказал «Известиям» руководитель научной экспертизы фонда Inbio Ventures (управляющая компания при венчурном инвестиционном фонде, который вкладывается в фармацевтические проекты) Илья Ясный. По словам эксперта, даже если компании будут продолжать снабжать участников препаратами, на всех их может просто не хватить.— Выход участников или даже исключение целого центра из исследований вполне возможны. Для этого достаточно написать дополнение к протоколу. Некоторые исследования могут быть долгими, и не факт, что запаса лекарств хватит до окончания всех сроков, — говорит Илья Ясный.
Несмотря на отсутствие юридических обязательств, отказ фармацевтических компаний от завершения уже начатых клинических исследований в России приведет к серьезным репутационным потерям, считает президент «Лиги защитников пациентов» Александр Саверский. У фармкомпаний есть этические кодексы, которые посвящены этим вопросам. Также существуют международные ассоциации исследователей и производителей лекарств, которые их контролируют.
— Если препарат помогает от серьезных заболеваний, например онкологических, то его использование становится жизненно важным для пациентов, принимающих участие в КИ. Если другая терапия не помогает, то они вынуждены надеяться только на тестируемое лекарство, — говорит Александр Саверский.Специалист также пояснил, что кроме предоставления участнику клинического исследования самого лекарства компания-устроитель оплачивает услуги врача-исследователя, который контролирует состояние пациента. Бросить участника без такого надзора нельзя, так как эффективность и безопасность препарата, который он принимает, еще не подтверждена. Если часть пациентов, участвовавших в КИ, умрет, то без помощи врача-исследователя об этом просто никто не узнает, так как участники могут проживать в разных местах. В таком случае жизнь остальных участников также окажется под угрозой.
КИ лекарственных средств — обязательный этап их сертификации за рубежом и в нашей стране, когда испытания проводятся на реальных пациентах. По действующим правилам для допуска на наш рынок зарубежных препаратов такие исследования должны обязательно проводиться в России. Их прекращение фактически говорит о том, что компании отказываются продавать новые виды лекарств у нас в стране.
Нужно отметить, что многие фармацевтические гиганты продолжают клинические исследования в России. Например, компания BIOCAD заявила, что текущие КИ в РФ будут продолжены в полном объеме, она не планирует приостанавливать действующие проекты и намерена ускорить старт испытаний новых препаратов, говорится в официальном заявлении фармацевтов. Продолжают исследования и многие другие зарубежные фармкомпании.
Ссылка на публикацию: iz.ru









